
Cara prof Miao, la mia mamma dice che puoi aiutarmi. Sul libro di scienze ho trovato scritto: “punto di congelamento o di fusione”. Ma scusa, a zero gradi l’acqua congela o si scioglie? Non sono due cose completamente diverse? Grazie se puoi rispondermi! PS: anche a me piacciono i gatti!
Oh, questi libri di scuola poco chiari! Ne ho una luuuunga esperienza. E se avessi avuto internet quand’ero studentessa, sarebbe stato fantastico: avrei capito, apprezzato, approfondito con molta più gioia e meno noia. Allora, vediamo quel è il mistero…

Cara prof Miao, la mia mamma dice che puoi aiutarmi. Sul libro di scienze ho trovato scritto: “punto di congelamento o di fusione”. Ma scusa, a zero gradi l’acqua congela o si scioglie? Non sono due cose completamente diverse? Grazie se puoi rispondermi!
Oh, questi libri di scuola poco chiari! Ne ho una luuuunga esperienza. E se avessi avuto internet quand’ero studentessa, sarebbe stato fantastico: avrei capito, apprezzato, approfondito con molta più gioia e meno noia.
Allora, andiamo per ordine.
L’acqua pura (senza residui, zuccheri, sali, eccc.) alla temperatura di 0°C e a pressione atmosferica si trova nel cosiddetto punto di congelamento o di fusione. Ma come, sembra una contraddizione! A 0 gradi si scioglie o diventa ghiaccio? Per non fondere i neuroni facciamo un passo alla volta. Immaginiamo di prendere un cubetto di ghiaccio e di metterlo in una vaschetta piena d’acqua e supponiamo anche che questa vaschetta sia perfettamente isolata dall’ambiente esterno in modo che non possa assorbire o cedere calore (mi viene in mente la barzelletta in cui si prendono in giro i fisici quando snocciolano le cosiddette “condizioni al contorno” cioè le condizioni alle quali avvengono gli esperimenti. C’è un fisico che deve aiutare un contadino perché le mucche hanno smesso di fare latte e inizia la spiegazione della soluzione dicendo “Supponiamo che la mucca sia una sfera…” scusate la divagazione!)
Supponiamo che all’inizio l’acqua si trovi a 10 gradi:
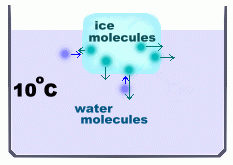
Le molecole dell’acqua allo stato liquido hanno più energia di quelle del cubetto, cioè la loro temperatura è maggiore: 10 gradi contro i 0 gradi del ghiaccio. Dato che c’è una differenza di temperatura, le leggi della termodinamica dicono che il sistema cubetto+acqua cercherà un equilibrio termico: con il passar del tempo la temperatura diventerà la stessa. Come quando ci proviamo la febbre: il termometro entra in equilibrio termico con l’ascella. Dunque cosa succede man mano che passa il tempo? Le molecole della superficie del cubetto vengono urtate da quelle più veloci dell’acqua e acquistano energia, quindi si staccano e il cubetto si riduce di volume. Ma se le molecole del cubetto acquistano, significa che qualcuno perde: sono le molecole dell’acqua, che trasferiscono energia durante gli urti. In altre parole la temperatura dell’acqua deve diminuire. A un certo punto il cubetto si è ridotto di dimensioni e l’acqua, che era a 10 gradi, arriva a 0 gradi. E qui succede qualcosa: apparentemente tutto si ferma.
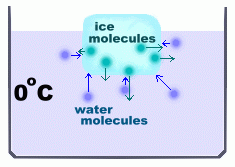
Ora tutto il sistema si trova a 0 gradi ed è in equilibrio dinamico: ci sono molecole che si staccano dal cubetto e molecole che dal liquido vanno a formare il cubetto. Il ritmo con cui l’acqua congela è lo stesso con cui il cubetto fonde: quindi 0 gradi è la temperatura di fusione/congelamento dell’acqua del sistema cubetto+acqua.
Cosa succede se, come avviene nelle bevande gassate, aggiungiamo zuccheri e gas?Riprendiamo la vaschetta cubetto+acqua in equilibrio dinamico (0 gradi) e aggiungiamo dello zucchero, 1 grammo per ogni litro d’acqua. Aggiungendo un estraneo, l’equilibrio si rompe. Le molecole di zucchero si mescolano all’acqua quindi attorno al cubetto gironzolano meno molecole d’acqua: ad attaccarsi al cubetto saranno meno numerose. In altre parole il ritmo di congelamento (numero di molecole d’acqua che si attaccano al cubetto nel tempo) diminuisce. Invece il ritmo di fusione (molecole che si staccano dal cubetto) rimane lo stesso perché gli urti continuano, anche da parte dello zucchero. Ma allora se la fusione rimane la stessa mentre il congelamento è più lento, alla fine il cubetto si scioglie. Come fare dunque per ripristinare le condizioni di equilibrio? Bisogna abbassare la temperatura del sistema e portarlo a -1,86 gradi, nel caso specifico… zuccherino! In queste condizioni, proprio come prima, il cubetto riceve energia dal liquido zuccherato e si scioglie un po’ ma allo stesso tempo un identico numero di molecole d’acqua si attaccano al cubetto. L’acqua salata è in equilibrio dinamico invece a -4 gradi. Ecco perché d’inverno si sparge il sale sulle strade per evitare che si formi il ghiaccio sull’asfalto o come mai se volete fare dei ghiaccioli alla cola, dovete avere un freezer che vada al di sotto di 0 gradi.
22 Febbraio 2022 il 23:36
Ottima spiegazione💪💪 voglio farle i miei complimenti; certo adatta spiegazione dai 12 anni a salire, altrimenti non tutti capirebbero. 🤔👍👍